Коррозия и защита от коррозииМеханизм химической коррозии
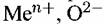 и электроны. Электрически заряженные частицы и электроны перемещаются в кристаллической решетке продуктов коррозии. Зона роста пленки связана со скоростью движения частиц. Если превалирует скорость диффузии ионов или атомов металла, то образование оксида происходит на внешней поверхности пленки. Наоборот, если сквозь пленку диффундирует главным образом кислород, то зоной роста пленки будет граница между пленкой и металлом. В и электроны. Электрически заряженные частицы и электроны перемещаются в кристаллической решетке продуктов коррозии. Зона роста пленки связана со скоростью движения частиц. Если превалирует скорость диффузии ионов или атомов металла, то образование оксида происходит на внешней поверхности пленки. Наоборот, если сквозь пленку диффундирует главным образом кислород, то зоной роста пленки будет граница между пленкой и металлом. В
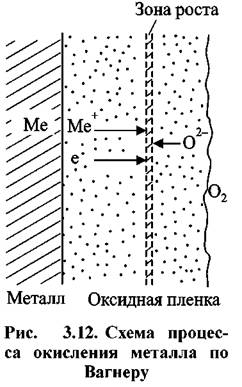
большинстве случаев скорости диффузии частиц соизмеримы, и тогда зона роста находится внутри пленки. Схематично это положение изображено на рис. 3.12.
Принято считать, что для большинства случаев основным направлением диффузии является движение атомов или ионов металла через пленку наружу, и, в меньшей степени, диффузия кислорода в обратном направлении.
Оксидные и солевые пленки на металлах имеют ионную кристаллическую структуру. Они обладают, как правило, ионной, а в некоторых случаях, и электронной проводимостью.
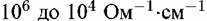 . Проводимость определяется движением свободных электронов. . Проводимость определяется движением свободных электронов.
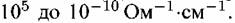 Движение электронов может быть обусловлено тепловой флуктуацией (п-проводи-мость) или перемещением связанных ковалентных электронов по вакантным местам (дыркам) валентной зоны (р-проводимость). Движение электронов может быть обусловлено тепловой флуктуацией (п-проводи-мость) или перемещением связанных ковалентных электронов по вакантным местам (дыркам) валентной зоны (р-проводимость).
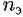 — число переноса электронов. Следует различать два типа направленного перемещения частиц в пленке: — число переноса электронов. Следует различать два типа направленного перемещения частиц в пленке:
движение ионов в сторону их меньшей концентрации, т.е. процесс диффузии;
перемещение ионов под влиянием электрического поля, или миграцию.
В таблице 3.4 приведены атомные и ионные радиусы некоторых элементов. Как показывают данные таблицы, ион металла имеет
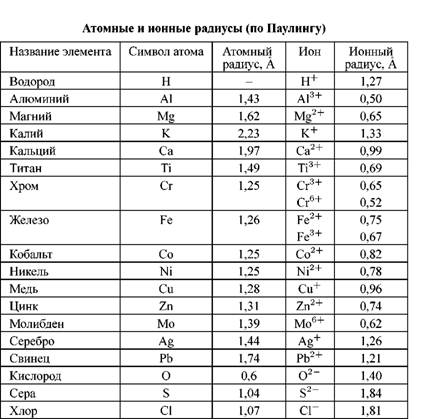
Таблица 3.4
меньший радиус, чем соответствующий атом металла. Следовательно, от металла сквозь пленку будут двигаться, в основном, ионы металла и электроны (см. рис. 3.12). Диффузия ионов кислорода происходит навстречу ионам металла. Ионизация кислорода при этом осуществляется на внешней поверхности пленки.
Радиус ионов металлов меньше, чем радиус иона кислорода. Поэтому металлические ионы имеют большую подвижность при диффузии и зона роста пленки сдвинута к внешней границе.
Диффузия в твердом теле при температурах ниже температуры плавления кристаллов может осуществляться по одному из двух механизмов:
движением атомов или ионов между узлами кристаллической решетки;
движением атомов или ионов через пустые узлы в решетке или по дислокациям и границам зерен.
Первый механизм (рис. 3.13) реализуется при образовании оксидов, ионы металлов которых имеют небольшие размеры по
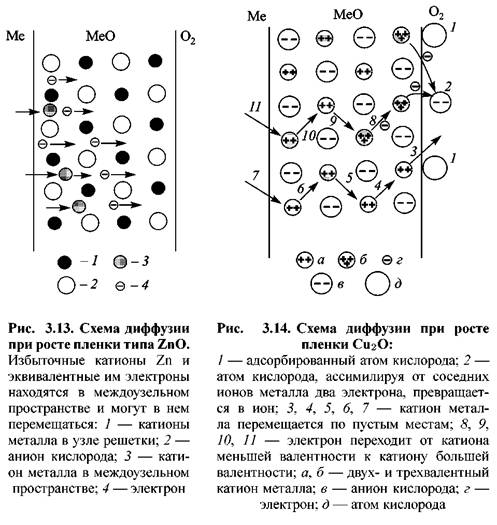

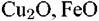 (рис. 3.14). При этом превалирует диффузия катионов металла и электронов через пленку наружу. (рис. 3.14). При этом превалирует диффузия катионов металла и электронов через пленку наружу.
В соответствие с приведенными механизмами различают два типа оксидов:
оксиды с избытком ионов металла по сравнению со стехиомет-рическим составом; эти оксиды увеличивают свою электропроводимость при нагреве в восстановительной атмосфере;
оксиды с избытком ионов кислорода по сравнению со стехио-метрическим составом; эти оксиды увеличивают электропроводимость при нагреве в окислительной атмосфере.
Ионно-электронная теория окисления металлов, которая сейчас наиболее признана, была разработана Вагнером. Им был выдвинут постулат о том, что в пленке происходит не только диффузия ионов за счет градиента концентраций, но осуществляется, главным образом, направленная миграция ионов в электрическом поле, создаваемом разницей потенциалов на внешней и внутренней поверхностях оксида.
Предполагалось, что процесс роста пленки — результат работы своеобразного гальванического элемента, у которого поверхность металла на границе с пленкой является анодом, т.е. поставляет катионы и электроны, а поверхность пленки на границе с реагентом — катодом, на котором атомы кислорода принимают электроны. Пленка, обладая смешанной ионно-электронной проводимостью, работает одновременно как внутренняя и внешняя цепь замкнутой ячейки.
Образовавшиеся на поверхности металла положительные ионы и электроны перемещаются в пленке раздельно.
Электроны перемещаются с большей скоростью. Диффузия ионов протекает в результате перемещения их по дефектным местам кристаллической решетки оксида.
Адсорбированные из газовой фазы молекулы кислорода диссоциируют на внешней поверхности оксида. Атомы кислорода, принимая электроны, превращаются в ионы О2-, которые начинают двигаться навстречу ионам металла. Таким образом, внешняя поверхность пленки, на которой кислород принимает электроны, является катодной поверхностью.
Встречная диффузия ионов металла и кислорода протекает в электрическом поле. Это означает, что уравнения кинетики и ее основные константы могут быть выведены, исходя из электрических параметров и закономерностей: величин ионной и электронной проводимости, чисел переноса ионов и электронов, закона Ома.
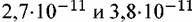
Константа скорости окисления тем больше при прочих равных условиях, чем больше изменение свободной энергии и чем выше удельная электропроводимость материала пленки. Если оксид обладает электроизолирующими свойствами, дальнейшее окисление не происходит. Этим объясняется, например, стойкость алюминия к процессам окисления.
|