Коррозия и защита от коррозииРастворение железа в кислых растворах
Для иллюстрации практического применения изложенных выше методов исследования электрохимических реакций рассмотрим механизм коррозии железа.
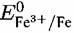 = —0,037 В. Поэтому при коррозии железа в = —0,037 В. Поэтому при коррозии железа в

Здесь рассматривается механизм, предложенный Бокрисом и получивший широкое распространение. Этот механизм не учитывает участия анионов раствора в процессе растворения и поэтому требует внесения существенных поправок, что будет показано ниже.
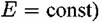 при при
увеличении рН на единицу (рис. 4.15). Другими словами, порядок анодной реакции растворения железа по ионам водорода равен — 1. Это с учетом найденного тафелевого наклона дает возможность принять следующую схему процесса.
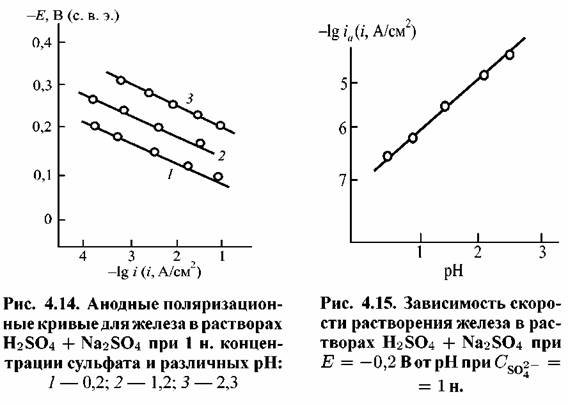
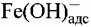
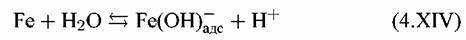
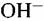 : :
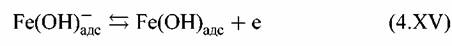
причем стадия (4.XV) предшествует замедленной стадии отщепления второго электрона и поэтому является равновесной. Стадия, лимитирующая скорость всего процесса, имеет вид:
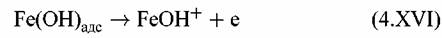
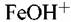 в растворе: в растворе:
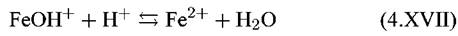
То, что схема (4.XIV)—(4.XVII) соответствует приведенным экспериментальным данным, вытекает из уравнения для скорости реакции, отвечающего этой схеме. С учетом замедленности стадии (4.XVI) для скорости растворения железа справедливо уравнение:
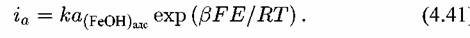 ) )
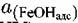 можно найти с помощью уравнения Нернста для можно найти с помощью уравнения Нернста для
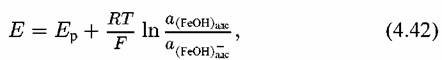
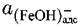 из уравнения диссоциации для стадии из уравнения диссоциации для стадии

Совместное решение уравнений (4.42) и (4.43) приводит к выражению:
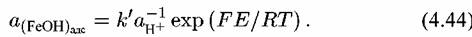 I I
Подстановка (4.44) в (4.41) дает уравнение для скорости растворения железа:

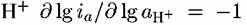 при Е = сопз! действительно совпадают с соответствующими экспериментальными значениями. при Е = сопз! действительно совпадают с соответствующими экспериментальными значениями.
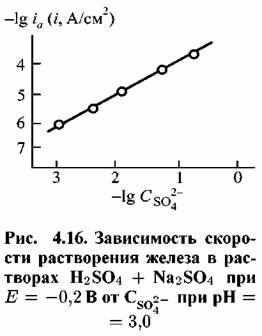
постоянных рН) и с ростом концентрации анионов раствора, например сульфата (рис. 4.16), причем порядок реакции по анионам близок к единице. Такой результат согласуется с предположением о том, что за рассмотренными выше стадиями (4.XIV) и (4.XV) следуют стадии
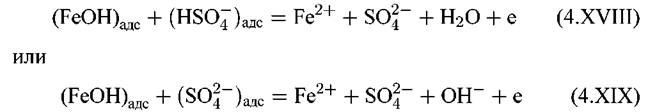
которые лимитируют скорость всего процесса. При этом совокупности последовательных реакций (4.ХТV), (4.XV), (4.ХVШ), а также (4.XIV), (4.XV), (4.XIX) протекают параллельно, так что для суммарной скорости растворения железа можно записать:
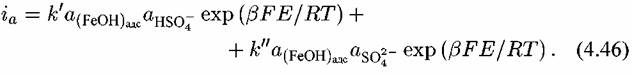
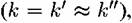 то уравнение (4.46) то уравнение (4.46)
можно переписать в виде:
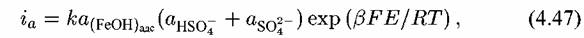
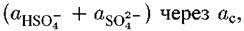 а также учитывая (4.XIV) и (4.XV) и логарифмируя, в виде: а также учитывая (4.XIV) и (4.XV) и логарифмируя, в виде:
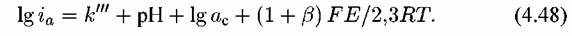
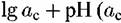 — суммарная аналитическая концентрация сульфата). — суммарная аналитическая концентрация сульфата).
|