Вязкость и пластичность нефтепродуктовВлияние состава жидкостей на зависимость их вязкости от температуры
Влияние химического состава сказывается в том, что при равных вязкостях температурный коэфициент вязкости разных жидкостей неодинаков. Различие между маловязкими жидкостями (а также при высоких температурах, которым отвечают низкие вязкости) невелико и часто близко к пределу точности измерения. С возрастанием вязкости оно увеличивается.
У равновязких высоковязких жидкостей отношение -^ может
различаться до десяти раз. Температурный коэфициент вязкости при критической температуре и соответственных температурах также зависит от состава жидкостей. Наконец, изменяемость
температурного коэфициента вязкости с температурой
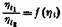 табл. 21). Сравнение вязкостно-температурной зависимости углеводородов и других основных компонентов нефтепродуктов в определенном интервале температуры (преимущественно 0—100° или 50— 100°) приводит к следующим общим выводам. табл. 21). Сравнение вязкостно-температурной зависимости углеводородов и других основных компонентов нефтепродуктов в определенном интервале температуры (преимущественно 0—100° или 50— 100°) приводит к следующим общим выводам.
Отношение возрастает в гомологических рядах одно типных соединений; температурный коэфициент вязкости не находится в такой простой зависимости от числа См-групп, как величина вязкости при постоянной температуре.
Вязкостно-температурные кривые нормальных и изопара-финов с одной изогруппой практически параллельны; по мере разветвления цепей вязкостно-температурный коэфициент возрастает и при наличии двух и трех изогруип превышает таковой у нормальных углеводородов .
Наличие двойных связей у алифатических углеводородов существенно не влияет на температурный коэфициент вязкости.
Циклические углеводороды обладают большим температурным коэфициентом вязкости, чем соответствующие алифатические
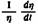 возрастает с повышением числа возрастает с повышением числа
колец в молекуле; переход ароматических колец в гидроароматические мало отражается на вязкостно-температурной зависимости 131, 32J.
Боковые алифатические цепи снижают температурный коэфициент вязкости циклических углеводородов; влияние боковой цепи возрастает с ее длиной; поэтому распределение атомов углерода в двух и большем количестве боковых цепей меньше отражается на вязкостно-температурной зависимости, чем если они все расположены в одной цепи.
Окисление и сульфирование углеводородов повышает их: температурный коэфициент вязкости.
На вязкостно-температурных кривых двух жидкостей, даже сильно различных по своему составу, можно найти точки с одинаковой для обеих жидкостей вязкостью. Понятно, что равным вязкостям соответствуют разные температуры. Портер установил интересное эмпирическое соотношение между такими точками Пусть первая жидкость имеет вязкость г при температуре 7, а вторая при Т2, тогда, как показал Портер, справедливо соотношение
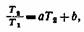
где а и Ь —постоянные величины. Как легко видеть, соотношение Портера выражает линейную зависимость отношения температур равных вязкостей от температур одной из них. Физический смысл этого отношения не ясен, но оно может быть полезным пр№ сравнении вязкостно-температурных свойств жидкостей.

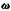 —константы. Величина w близка к постоянной Ь уравнения Ван-дер-Ваальса. —константы. Величина w близка к постоянной Ь уравнения Ван-дер-Ваальса.
Из формулы (IV, 1) следует, что

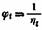 и введя обозначения и введя обозначения
 (IV, 1а) можно написать в виде (IV, 1а) можно написать в виде
откуда следует, что текучесть является линейной функцией удельного объема. В координатах текучесть — удельный объем на графике получаются прямые линии.
Формуле А. И. Бачинского хорошо подчиняются низкомолекулярные и маловязкие жидкости. Вода и бензол относятся к немногим исключениям.
Весьма существенно, что физические свойства, характеризующие структуру большинства жидкостей, подчиняющихся закону А. И. Бачинского, связаны с температурой аналогичными закономерностями. Мак-Леод обратил внимание на обратную зависимость в гомологических рядах между коэфициентом вязкости и так называемым свободным пространством между молекулами, или коэфициентом термического расширения жидкостей . Его формула является другим способом выражения уравнения А. И. Бачинского, и наблюдавшаяся зависимость непосредственно вытекает из соотношения (IV, I), выражающего связь между вязкостью и удельным объемом.
Работа Мак-Леода была опубликована на 10 лет позднее исследований А. И. Бачинского, предложенное им уравнение по форме менее удачно, чем уравнение А. И. Бачинского. Между тем необходимо отметить, что в статье Мак-Леода нет ссылок на работу А. И. Бачинского и в иностранной литературе закон, связывающий вязкость с плотностью или с аналогичным показателем строения жидкости, часто неосновательно называется законом Мак-Леода.
Высокомолекулярные и высоковязкие жидкости (в том числе минеральные масла и масляные углеводороды, жидкие смолы и высшие нафтеновые кислоты) не подчиняются уравнению Бачин-ского. Вязкость таких жидкостей очень сильно зависит от температуры. Многие из них также обладают аномальной температурной зависимостью плотности и коэфициента термического расширения.
Для объяснения этих особенностей было сделано предположение, что между молекулами этих жидкостей возникают более или менее прочные связи—происходит ассоциация молекул. Возникновение дополнительных связей между молекулами, помимо постоянно действующих сил сцепления (когезии), приводит к повышению сопротивления тангенциальному сдвигу, т. е. в конечном итоге к росту вязкости. Кроме того, следует указать, что объем группы ассоциированных молекул больше, чем сумма объемов отдельных молекул, входящих в группу, так как в нее включается и межмолекулярное пространство. Возрастание объема, занятого молекулами, также обусловливает повышение вязкости жидкости. Соотношение между ассоциированной и неассоциированной частями жидкости зависит от температуры: чем ниже температура, тем больше ассоциация. Таким образом, температурная зависимость вязкости определяется двумя факторами: удельным объемом и ассоциацией молекул.
Исходя из вискозиметрических данных, были предприняты многочисленные попытки вычислить степень ассоциации (см., например, ). Однако вопрос об ассоциации жидкостей недостаточно ясен. Прежде всего нельзя делать заключение о природе жидкости на основании отклонения от одной, хотя бы даже и весьма важной и удобной, эмпирической формулы. Такая формула является не чем иным, как формальным математическим описанием экспериментально установленных зависимостей. А. И. Бачинский отметил , что если пользоваться эмпирической формулой вязкости другого вида (см. формулу (IV, 13)], то некоторые так называемые ассоциированные жидкости окажутся неассоциированными. Заметим, однако, что в последнее время формула (IV, 1) нашла и теоретическое обоснование.
Забиваем Сайты В ТОП КУВАЛДОЙ - Уникальные возможности от SeoHammer
Каждая ссылка анализируется по трем пакетам оценки: SEO, Трафик и SMM.
SeoHammer делает продвижение сайта прозрачным и простым занятием.
Ссылки, вечные ссылки, статьи, упоминания, пресс-релизы - используйте по максимуму потенциал SeoHammer для продвижения вашего сайта.
Что умеет делать SeoHammer
— Продвижение в один клик, интеллектуальный подбор запросов, покупка самых лучших ссылок с высокой степенью качества у лучших бирж ссылок.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз,
а первые результаты появляются уже в течение первых 7 дней.
Зарегистрироваться и Начать продвижение
Более правильно делить жидкости, как это и предлагает А. И. Бачинский, на нормальные и ненормальные, или аномальные, относя к первым такие, которые подчиняются его формуле. К тому же в настоящее время существует еще очень мало прямых не вискозиметрических данных о молекулярной ассоциации жидкостей, изменении ассоциации с температурой и давлением, а также о величине и природе сил, обусловливающих это явление.
Не вызывает сомнения, однако, что вязкие нефтепродукты, смолы, растительные жиры, жидкие жирные кислоты, расплавленные стекла, вода и подобные жидкости имеют сложную структуру и силы молекулярного взаимодействия превышают силы, вычисленные из обычных молекулярно-кинетических представлений. Доказательство такой структуры мы находим в рентгенографических исследованиях жидкостей В. И. Данилова , И. В. Радченко и в некоторых других работах .
В этом отношении вода исследована более подробно, чем другие аномальные жидкости. Аномальную температурную зависимость многих ее свойств объясняли возникновением еще в жидком состоянии квазикристаллических образований (теория Стюарта). Когда эта теория не нашла подтверждения, была выдвинута гипотеза об ассоциации молекул воды в виде так называемых гидролей типа (НаО)а, (НаО)8 и т. д. Степень этой неустойчивой полимеризации определяется температурой. Однако в свете последних данных более вероятно, что молекулы воды ассоциируются за счет водородных связей1, образуя термически неустойчивые комплексы тетраэдрической формы.
При взаимодействии молекул углеводородов большую роль играют ван-дер-ваальсовы силы. В нефтепродуктах со смолами и другими кислородсодержащими соединениями на ассоциацию могут влиять водородные связи и взаимодействие поляризованных молекул. Возможно, что одним из факторов ассоциации высокомолекулярных углеводородов является энтропия, связанная с большей вероятностью взаимно параллельной ориентацией длинных цепей таких молекул.
|