Вторичная переработка полимеровПолиэфиры
Полиэфиры являются полимерами, содержащими повторяющиеся эфирные группы в скелете цепи; они подразделяются на полиэфиры типов ЛАВВ и АВ, когда они произведены, соответственно, из гликолей и двухосновых кислот (или их производных) и оксикислот (или лактонов).
Среди различных типов полимеров полиэфиры наиболее просты в химической переработке, потому что эфирные мостики полимерных цепей легко вступают в реакцию с различными нуклеофильными реагентами (такими как вода, спирты, гликоли и др.), давая высокий выход полезных продуктов. Хотя все полиэфиры могут быть переработаны по этой схеме, на практике ПЭТ является единственным полиэфиром, подвергаемым вторичной переработке ввиду простоты сбора и огромного количества использованных бутылок, волоконного утиля и фотопленок. Поэтому ниже мы подробно рассмотрим химическую переработку ПЭТ, хотя подход может быть распространен на любой другой полиэфир. В литературе описано множество технологий химической переработки бывшего в употреблении ПЭТ (преимущественно это патенты), но большинство технологий очень похожи друг на друга, и в последующих разделах мы выберем для обсуждения характерные примеры возможных подходов, но не будем приводить обзор литературы.
ПЭТ обычно получают полимеризацией этиленгликоля (ЭГ) с терефталевой кислотой (ТК) или ее диметилэфиром (ДМТ); реакция проводится в два этапа в соответствии с уравнениями (10.1а), (10.1b) и (10.2).
Если на первом этапе используется ТК, то реакция (10.1а) обычно проводится при 180-210 °С, под давлением, без катализатора; если на первом этапе используется ДМТ, то реакция (10.16) проводится при 150-210С, при атмосферном давлении и в присутствии катализатора (как правило, ацетатов Са, Zn, Мп). Обе реакции являются равновесными с низкими константами равновесия (< 1), и поэтому вода и метанол (МеОН) должны постоянно удаляться для сдвига равновесия в сторону необходимых продуктов. В обоих случаях используется большой молярный избыток ЭГ относительно стехиометрического количества ТК или ДМТ (1,8 и 2,2 молей ЭГ на моль ТК или ДМТ, соответственно) [4].

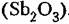 . Константа равновесия в этом случае также низкая и ЭГ должен эффективно удаляться, чтобы получить ПЭТ с высокой молекулярной массой. . Константа равновесия в этом случае также низкая и ЭГ должен эффективно удаляться, чтобы получить ПЭТ с высокой молекулярной массой.
Благодаря низким константам равновесия, сравнительно просто сдвинуть равновесие реакций (10.1а), (10.16) и (10.2) в направлении реагентов и получить мономеры ТК, ДМТ, ЭГ и бис-оксиэтилтерефталата (БОЭТ) за счет реакции ПЭТ с избытком воды, МеОН или ЭГ. Введение катализатора (ацетаты Са, Zn, Мn, алкоксидов титана или оловосодержащих соединений) может потребоваться для уменьшения продолжительности реакции.
Важно отметить, что ЕВА одобрила использование чистых мономеров, полученных деполяризацией ПЭТ, для производства нового ПЭТ, который разрешено использовать в контакте с пищевыми продуктами.
Низкомолекулярные продукты (не мономеры), которые можно использовать в виде промежуточных субстанций в различных химических процессах, получаются, если для разложения цепей ПЭТ спирты, аммиак, амины и т. д. применяются в большом избытке; ниже приводится несколько примеров.
Смесь олигомеров, которая получается в конце первого этапа или при более высокой средней молекулярной массе, образуется при добавлении небольших количеств ЭГ и воды. Эти олигомеры можно использовать вновь для приготовления ПЭТ, вводя их непосредственно во второй этап процесса полимеризации. Олигомерные сополимеры можно добавлять при использовании иных, нежели ЭГ, гликолей для деполимеризации ПЭТ. Их можно применять для изготовления ненасыщенных полиэфиров, ПУ, красок, адгезивных средств и т. д.
Различные технологические подходы к химической переработке ПЭТ подробно рассмотрены ниже.
|